细胞治疗服务
支持您的细胞治疗生产需求
您是否希望使用STEMCELL产品作为辅助材料(AM)或原材料来生产细胞治疗产品?通过我们的细胞治疗服务项目,我们可以与您合作开发满足您特定需求的解决方案,例如定制产品开发、更高合规性的产品生产、监管支持和定制化文件支持等。
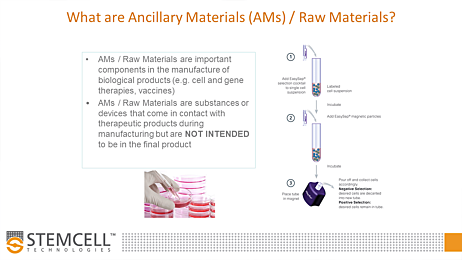
在细胞治疗服务项目下,STEMCELL可能能够支持在批准的研究性新药(IND)申请、临床试验授权/申请(CTA)或等效的监管文件下,将我们的产品作为AM(定义见USP第<1043>章或Ph. Eur5.2.12通则)1,2。我们已经成功支持了全球超过45项临床试验。
个性化支持和定制解决方案

您将与指定的细胞治疗服务项目经理合作,开始讨论您的定制需求。这些专家经过培训,可以提供有关STEMCELL服务和能力的信息和反馈,并全面了解您的需求,以便设计出的最佳解决方案来满足您的需求。
在项目设计阶段的初期,您的项目经理将与来自多个部门(如研发、生产、工艺开发、质量控制、质量保证和监管事务)的经验丰富的员工组成的跨职能团队进行协作,以确保项目目标的准确设计。在签订相关的合同和保密协议后,项目将进入实施阶段,届时将为您的项目分配一个专门的团队。
细胞治疗服务项目经理将指导您完成这一协作过程,并将成为您的唯一联系人。从项目启动到完成,项目经理将确保您随时了解项目的进展,并且确保项目按时交付、在预算内并符合您所要求的质量标准。
为什么选择与我们合作?
- 我们与世界各地的客户合作,以满足其国家或地区特定的监管要求。
- 我们严格的供应商资质认证与管理流程可确保材料和服务持续保持高质量标准,并提供稳定可靠的供应保障。
- 我们能为您的工作流程从头到尾地提供创新的、专业的试剂。
- 我们在符合相关cGMP标准的条件下进行部分产品的内部生产和测试,并具备在USP <1043>或Ph. Eur. 5.2.12下支持AM资格认证的能力。
- 我们的认证地分销中心网络能够全球配送我们的产品。
在我们的细胞治疗服务团队的支持下,我们可帮助您应对复杂的定制化监管要求。请联系您当地的STEMCELL代表,开始讨论您的特定法规或产品要求,或使用下方表格。
其他资源
参考文献
- General Chapter <1043> Ancillary materials for cell, gene, and tissue engineered products. (2017) In: The United States Pharmacopeia.
- Chapter 5.2.12. Raw materials for the production of cell-based and gene therapy medicinal products. In: European Pharmacopeia.

 EasySep™小鼠TIL(CD45)正选试剂盒
EasySep™小鼠TIL(CD45)正选试剂盒










 沪公网安备31010102008431号
沪公网安备31010102008431号